1.仿硒酶工程研究
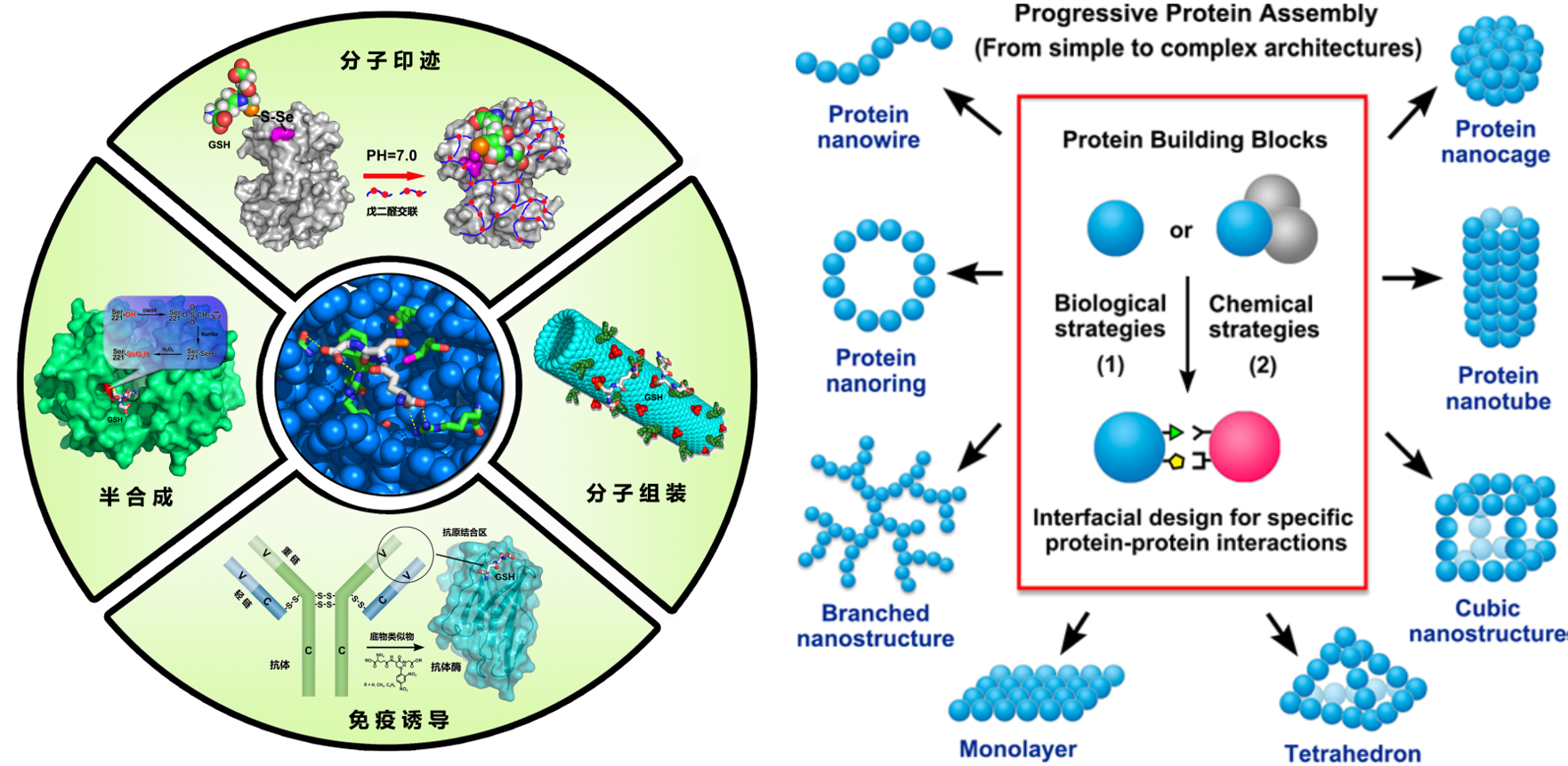
围绕构筑高效仿酶体系,揭示生物酶催化本质等重要科学问题,开展了系统的仿硒酶工程研究。建立和发展了分子自组装与仿酶相结合的新技术和新方法,获得了多酶功能协同的超分子仿酶体系,实现了多酶的功能协同。(1)在分子水平构筑了分子识别与催化协同的智能仿硒酶体系。在变构蛋白上精确构筑了硒酶识别和催化中心,利用蛋白质的构象变化成功实现了对底物识别特异性的控制,从而实现了对硒酶活性的可逆调控(参见Angew. Chem. Int. Ed. 2014, 53, 13536)。(2)在构筑蛋白质超分子聚合物解决硒酶稳定性方面取得重要成果。利用金属螯合作用和多重非共价作用网的协同驱动,实现了对蛋白质组装方向的精确控制(参见JACS. 2013, 135, 10966; ACS nano, 2015, 9, 5461)。通过主客体相互作用,构建了活力在天然酶水平的蛋白质超分子聚合物纳米线,通过稳定蛋白质的构象成功解决了酶稳定性问题(参见Angew. Chem. Int. Ed. 2013, 52, 5590)。(3)在超分子水平上构筑多酶协同的蛋白质组装体方面取得重要成果。我们发展了电荷相互作用驱动的蛋白质组装新方法。利用环状蛋白质与量子点、树枝状分子以及聚合胶束的多重静电作用,成功实现了多酶的协同及多酶的功能集成(参见ACS Catal. 2020, 10, 9735;Angew. Chem. Int. Ed. 2014, 53, 9343;ACS Nano, 2017, 11, 938)。
2.新型纳米结构用于构建人工光合作用系统
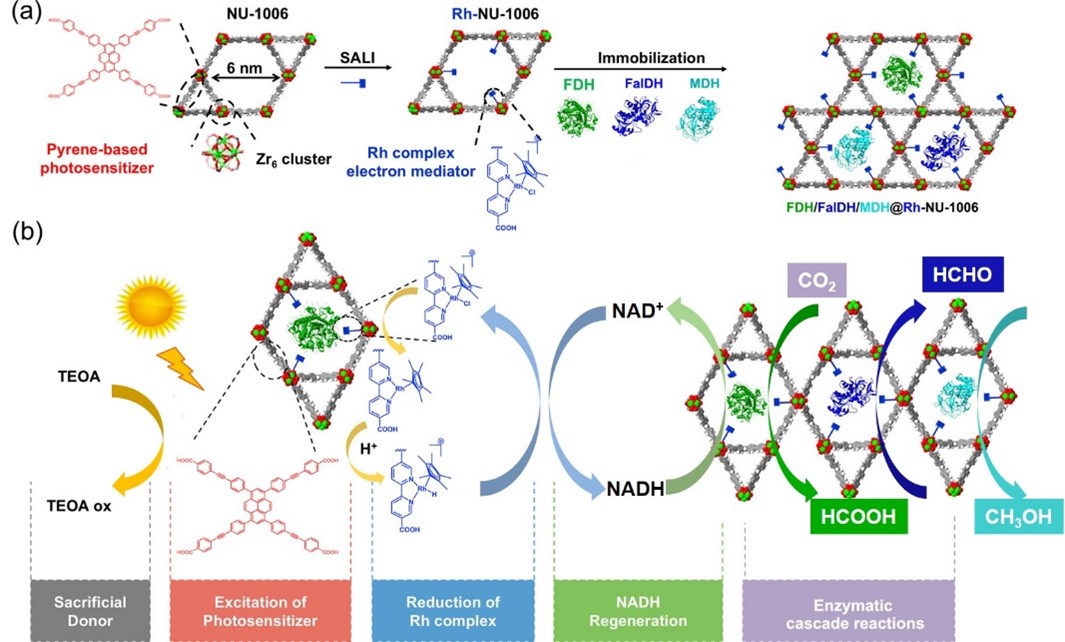
环境污染和能源短缺已经是制约人类可持续发展的巨大障碍。二氧化碳(CO2)的资源化利用,是缓解化石能源枯竭和温室效应这两大问题的有效途径之一。受天然光合作用启发,利用太阳能作为能量来源,将生物材料优异的光捕获能力与生物体系优异的催化能力相结合,构建人工合成或半人工光合作用体系,是未来实现二氧化碳资源利用有效的手段。通过创制高效的人工光捕获系统和高光催化活性的CO2还原酶,实现构筑高效人工光合CO2还原体系。该策略也为构建高效光合产氢及光合产氧系统提供思路。
3.仿生离子通道的设计与制备
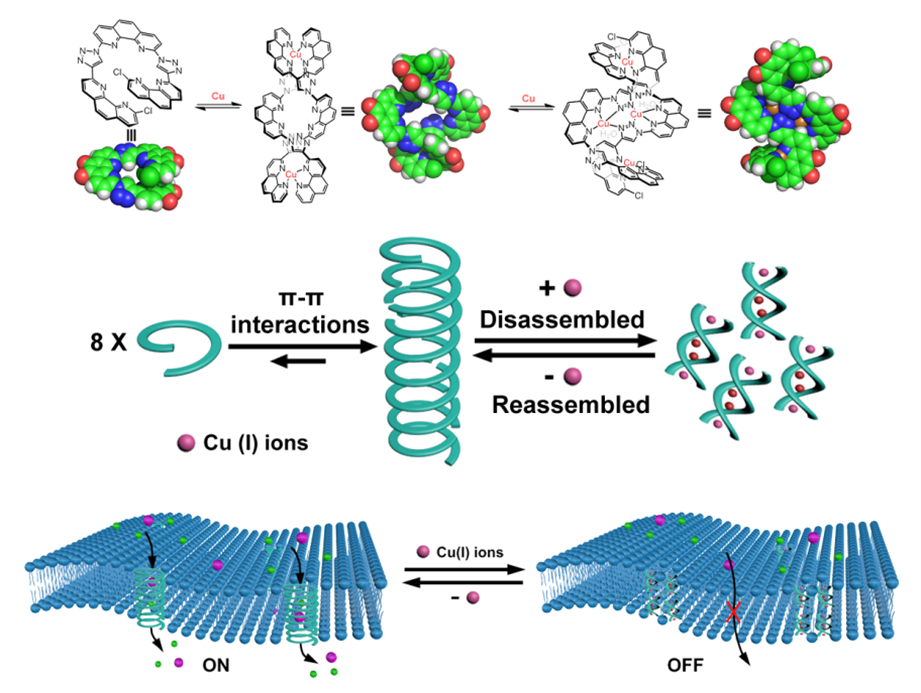
利用化学合成体系来构建人工离子通道并复制天然离子通道的功能仍面临巨大挑战。受天然KcsA K+通道的启发,利用π-π堆叠驱动力设计合成了高度自折叠的螺旋折叠体,其内部含有多个离子结合位点的含纳米孔的螺旋折叠体,利用超分子组装技术实现了含孔螺旋折叠体寡聚物的嵌膜组装,构筑了高效的仿生离子通道(Angew. Chem. Int. Ed. 2016, 55, 9723 )。进一步调控通道内径,并使通道内部离子结合位点进行线性连续排列,从而实现了通道内部结合位点的相互作用的连续性,构筑了一种新型的高选择性的人工离子通道,实现了通道跨膜传输钾离子的高效性与专一性。该研究成果发表在Angew. Chem. Int. Ed. 2017, 56, 12668-12671上。通过精确设计了具有铜离子调控含孔道单螺旋和无孔道双螺旋互变行为的芳香螺旋寡聚物,利用具孔道单螺旋自发形成的一维自组装螺旋管,将该通道嵌入磷脂双分子层,通过铜离子配位与去配位诱导单双螺旋结构互变进而导致的自组装螺旋管的解组装和重新组装,实现了所设计离子通道的可逆关闭与打开,发展了高效、稳定的科开关的智能型人工离子通道(Angew. Chem. Int. Ed. 2020, 59, 13602 –13607)。
4.仿光捕获系统研究
设计制备光捕获系统是模拟自然光合作用的重要步骤。我们以蛋白质组装为手段,发展了系列构筑一维、二维到三维的蛋白质组装体的新方法,构筑了不同层次和结构的蛋白质组装体及智能化蛋白质组装体,实现了多种刺激对蛋白质组装体结构的调控。基于蛋白质组装策略设计制备了一系列人工光捕获系统,实现了高效荧光共振能量转移。例如,通过计算机模拟和基因工程辅助,利用温和的酶催化方法共价组装,设计并制备了规则有序的二维蛋白质片层纳米阵列。受到自然界中色素分子分布在片层结构的类囊体膜上这一特点的启发,我们将具有尺寸依赖性的正电荧光量子点通过静电相互作用有序排布到蛋白片层表面,实现高效荧光共振能量转移,同时有效避免了聚集淬灭的发生。该工作发表在ACS Nano, 2017, 11, 938-945上;发展了利用胶束诱导蛋白质自组装的新方法。利用有序的给体和受体排布模拟光俘获系统,实现了高效的能量传递(参见ACS Nano 2016, 10, 421-428,ACS nano, 2019, 13, 1861-1869)。在蛋白质组装及功能化研究方面,应邀撰写了的综述(Chem. Rev. 2016, 116, 13571-13632;Chem. Soc. Rev., 2016, 45, 2756-2767)。